Методики регистрации биопотенциалов
Биопотенциал (биоэлектрический потенциал, устар. биоток) – обобщенная характеристика взаимодействия зарядов, находящихся в исследуемой живой ткани, например, в различных областях мозга, в клетках и др. структурах.
Измеряется не абсолютный потенциал, а разность потенциалов между двумя точками ткани, отражающая ее биоэлектрическую активность, характер метаболических процессов. Биопотенциал используют для получения информации о состоянии и функционировании различных органов.
Биоэлектрические явления в тканях – это разность потенциалов, которая возникает в тканях в процессе нормальной жизнедеятельности. Эти явления можно регистрировать, используя трансмембранный способ регистрации. При этом один электрод располагается на наружной поверхности клетки, другой – на внутренней.
При таком способе регистрируются:
— потенциал покоя или мембранный потенциал;
Методы регистрации биопотенциалов:
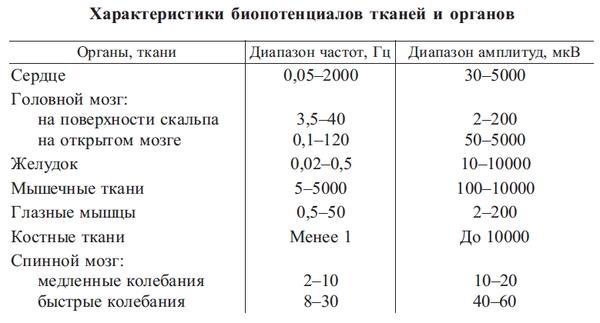
1. Электроэнцефалография (ЭЭГ) – метод регистрации электрической активности (биопотенциалов) головного мозга. Разность потенциалов, возникающая в тканях мозга, очень мала (не более 100 мкВ), и потому может быть зарегистрирована и измерена только при помощи специальной электронно-усилительной аппаратуры – электроэнцефалографов Применение электроэнцефалографии помогает определить локализацию патологического очага, а нередко и характер заболевания.
2. Реовазография – метод изучения сосудистой системы с использованием высокочастотного переменного тока для определения сопротивляемости участков тела. В момент притока крови сопротивление увеличивается и регистрируется кривая, совпадающая со сфигмограммой (записью пульса), но отличающаяся от последней формой. В неврологической практике часто производят реовазографию конечностей (при радикулите, неврите, невралгии, полиневрите и т. д.).
3. Эхоэнцефалография является важным методом диагностики объемных процессов головного мозга (опухоли, кисты, эпи- и субдуральные гематомы, абсцессы) и основан на принципе ультразвуковой локации – направленные в мозг короткие ультразвуковые импульсы отражаются от его внутренних структур и регистрируются.
Эхоэнцефалограмму (ЭхоЭГ) получают с помощью эхоэнцефалографа, снабженного специальным пьезоэлектрическим датчиком, работающим в двойном режиме – излучателя и приемника ультразвуковых импульсов, регистрируемых после возвращения на экране осциллографа.
4. Электромиография – это метод регистрации колебаний биопотенциалов мышц для оценки состояния мышц и нейродвигательного аппарата в покое, при активном расслаблении, а также при рефлекторных и произвольных движениях. С помощью электромиографии можно выявить, связано ли изменение электрической активности с поражением мотонейрона или синаптических и надсегментарных структур.
Электромиографические данные широко используются для уточнения топического диагноза и объективизации патологических или восстановительных процессов. Высокая чувствительность этого метода, позволяющая выявлять субклинические поражения нервной системы, делает его особенно ценным.
В период функциональной активности нервов и мышц возникают чрезвычайно слабые (от миллионных до тысячных долей вольта), быстрые (тысячные доли секунды) и частые колебания электрического потенциала.
Электромиография широко применяется не только в неврологической практике, но и при изучении поражения других систем, когда возникают вторично обусловленные нарушения двигательной функции (сердечно-сосудистые, обменные, эндокринные заболевания).
Дата добавления: 2018-04-04 ; просмотров: 728 ; ЗАКАЗАТЬ РАБОТУ
источник
Электромиография
Электромиография — метод исследования двигательного аппарата, основанный на регистрации биопотенциалов скелетных мышц. Электромиографию используют в хирургической и ортопедической стоматологии, ортодонтии, стоматоневрологии как функциональный и диагностический методы для исследования функций периферического нейромоторного аппарата оценки координации мышц челюстно-лицевой области во времени и по интенсивности, в норме и при патологии — при травмах и воспалительных заболеваниях челюстно-лицевой области, аномалиях прикуса, миопластических операциях, дистрофиях и гипертрофиях жевательных мышц, расщелинах мягкого неба и других заболеваниях.
ФИЗИЧЕСКИЕ И ФИЗИОЛОГИЧЕСКИЕ ОСНОВЫ ЭЛЕКТРОМИОГРАФИИ
Сокращение мышечной ткани вызывается потоком импульсов, возникающих в различных отделах центральной нервной системы и по двигательным нервам распространяющихся в мышцы. Возбуждение двигателе ной единицы нейромоторного аппарата проявляется генерацией потенциалов действия с интегральным выражением отдельных мышечных волокон. Возбуждение мышечной ткани представляет сложный комплекс явлений, складывающихся из усиления обменных процессов, повышения теплопродукции, из специфической деятельности (сокращение мышечных волокон), изменения электрического потенциала в возбужденном участке мышц. Для целей электромиографии непосредственный практический интерес представляет изменение электрического потенциала мышечного волокна.
В возникновении электрических (мембранных) потенциалов решающую роль играют изменение ионной проницаемости клеточных мембран, регуляторные механизмы этого процесса, ионы натрия и калия, а также хлора и кальция. На примере функции так называемого натрий-калиевого насоса можно рассмотреть механизм возникновения потенциалов покоя и действия мышечной клетки.
Потенциал покоя обусловлен функцией насоса клетки, т. е. движения ионов натрия из клетки в межклеточную жидкость, а ионов калия из нее внутрь клетки через клеточную мембрану. Следствием этого перехода является изменение концентрации ионов в клетке и возникновение ЭДС. Схема возникновения потенциала действия мышечной клетки такова: под воздействием раздражителя (нервного импульса) резко повышается проницаемость мембраны мышечной клетки для ионов натрия (примерно в 20 раз больше, чем для ионов калия). Вследствие значительного различия концентрации ионов натрия и калия в эту фазу деполяризации мембрана мышечной клетки становится заряженной отрицательно (фаза деполяризации). Вторая фаза (фаза реполяризации) обусловлена инактивацией натрий-калиевого насоса: движение ионов натрия из межклеточной жидкости в клетку прекращается. При воздействии последующих нервных импульсов цикл фаз де- и реполяризации повторяется. Таким образом, разность концентраций ионов натрия и калия в мышечной клетке обусловливает возникновение ЭДС — потенциалов покоя и действия, которые с помощью электродов, электронных усилителей и регистраторов можно записать графически.
С помощью электромиографии регистрируют изменения разности потенциалов внутри или на поверхности мышцы, возникающие в результате распространения воз-
Суждения по мышечным волокнам. Регистрируемые изменения разности потенциалов (или биоэлектрическую активность) мышц называют электромиограммой (ЭМГ).
Электромиография основана на регистрации потенциалов действия мышечных волокон, функционирующих в составе двигательных единиц (ДЕ). ДЕ — функциональная единица произвольной и рефлекторной активности мышцы. Она состоит из мотонейрона и группы мышечных волокон, иннервируемых этим мотонейроном (рис. 43).
Мышечные волокна, входящие в одну ДЕ, возбуждаются и сокращаются одновременно в результате возбуждения мотонейрона. Количество, мышечных волокон, иннервируемых одним мотонейроном, т. е. входящих в одну ДЕ, неодинаково в различных мышцах. В собственно жевательных мышцах на один мотонейрон приходится 100 мышечных волокон, в височной — 200; в мимических мышцах ДЕ более мелкие, они включают до 20 мышечных волокон. В небольших мимических мышцах это соотношение еще меньше; таким образом, обеспечивается высокий уровень дифференциации сокращений мимических мышц, обусловливающих широкую гамму мимики лица.
В состоянии покоя мышца не генерирует потенциалов действия, поэтому ЭМГ расслабленной мышцы имеет вид изоэлектрической линии. В результате прохождения импульсов от мотонейронов по нерву через нервно-мышечные окончания происходит возбуждение ДЕ, которое можно зарегистрировать игольчатым электродом в виде потенциала действия ДЕ, являющегося алгебраической суммой потенциалов действия отдельных мышечных волокон. Потенциал действия отдельной ДЕ обычно имеет вид 2—3-фазного колебания с амплитудой 100—3000 мкВ и длительностью 2—10 мс (рис. 44).
Увеличение силы сокращения мышцы возникает вследствие увеличения числа работающих ДЕ и частоты их разрядов. На ЭМГ этот процесс выражается в увеличении частоты и амплитуды колебаний, в результате временной и пространственной суммации потенциалов действия ДЕ (рис. 45). Такую ЭМГ называют интерференционной. Накожными электродами обычно регистрируют интерференционную ЭМГ, т. е. активность большого числа ДЕ участка мышцы, расположенного вблизи электродов, суммированную во времени и в пространстве. Условия пространственной суммации потенциалов действия ДЕ (т. е. пространственное расположение мышечных волокон), различная удаленность «генераторов» биопотенциалов от регистрирующих электродов являются одним из факторов, определяющих параметры регистрируемой ЭМГ. ЭМГ отражает степень моторной иннервации, косвенно свидетельствует об интенсивности сокращения отдельной мышцы и дает точное представление о временных характеристиках этих процессов.
Различают три основных вида электромиографии:
- 1) интерференционная электромиография (синонимы:, поверхностная, суммарная, глобальная), проводят ее посредством отведения биопотенциалов мышц, накладывая электроды на кожу, площадь отведения большая;
- 2) локальная электромиография — регистрацию активности отдельных ДЕ осуществляют с помощью игольчатых электродов;
- 3) стимуляционная электромиография — производят регистрацию электрического ответа мышцы на стимуляцию нерва, иннервирующего эту мышцу.
Поскольку запись ЭМГ является результатом совокупной деятельности мышцы как источника биопотенциалов и аппаратуры, с помощью которой отводят и регистрируют эти биопотенциалы, следует учитывать влияние методических условий на процесс регистрации ЭМГ.
источник
Прибор для регистрации биоэлектрических потенциалов человека
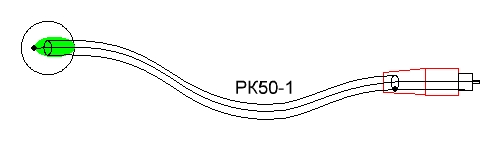
Строго говоря, с медицинской точки зрения описываемое «устройство» нельзя называть «прибором» — оно имеет всего два измерительных электрода и один «земляной», но при подключении к звуковой карте компьютера позволяет регистрировать сигналы амплитудой от 10 мкВ в диапазоне частот от 4 до 20 Гц (по уровню -3 dB). В эти рамки попадают некоторые биопотенциалы, снимаемые при электроэнцефалографии, электрокардиографии и электромиографии [1] (рис.1) и поэтому, для краткости, позволю себе по ходу текста называть его «прибором». Всё-таки, он собирался с прицелом на просмотр альфа-ритмов головного мозга :-), но первоначальная идея в связи с общей сложностью задуманного проекта ни во что не воплотилась и постепенно заглохла, а прибор далее благополучно применяется для контроля сердечной активности при физических тренировках.
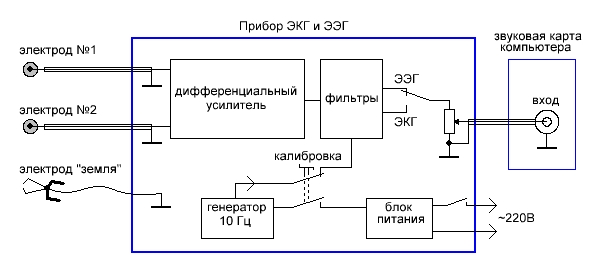
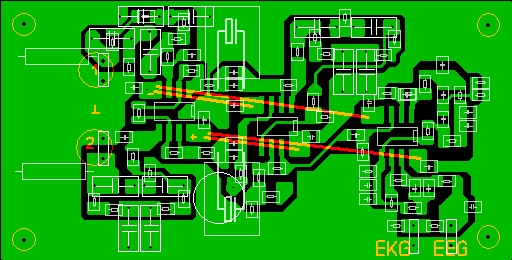
Никаких цифровых фильтров и цифровых обработок в тракте прохождения сигналов нет — только аналоговые. Электрические импульсы, снимаемые электродами с поверхности тела человека, усиливаются, фильтруются и подаются в компьютер (рис.2), где визуализируются (о, какое слово. :-)) при помощи программ SpectraLAB или SpectraPLUS. Сервис этих программ позволяет просматривать полученные данные как в реальном времени, так и в записи.
Рис.2
В основу прибора сначала был взят принцип, использованный Adam Overton [2], но, как обычно это происходит, сначала схемотехника была изменена под наличествующую элементную базу, а затем и совсем переработана. Кроме этого, калибровочный генератор собран на цифровой микросхеме, а питание схемы сделано от сети 220В. Всё устройство конструктивно выполнено в одном корпусе (рис.3) размерами 200х100х45 мм.
Рис.3
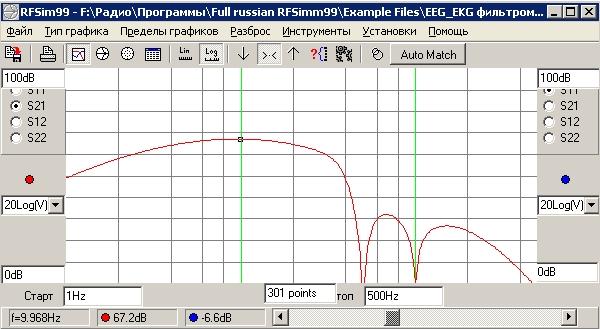
Максимальное усиление тракта на частоте 10 Гц около 67 dB (более 2200 раз). График АЧХ, не учитывающий подавление синфазных сигналов во входном инструментальном усилителе, рассчитан в программе RFSim99 и приведён на рисунке 4. Нижняя граница частот регистрации обусловлена пропускной способностью входной цепи компьютера (обычно это 5-10 Гц по уровню -3 dB). Верхняя же граница частот ограничена искусственно (для подавления помехи 50 Гц) и имеет на 20 Гц спад -3 dB, на 30 Гц около -6 dB, а 40 Гц ослаблены на 18 dB (в 9 раз относительно 10 Гц). Частота 50 Гц подавлена примерно на 40 dB (100 раз) относительно уровня, приходящего на вход.
Рис.4
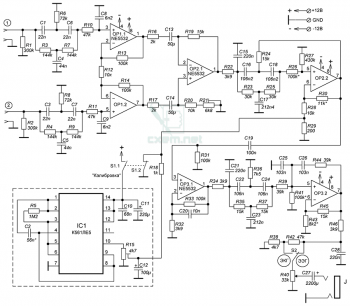
Электрическая схема приведена на рисунке 5. На операционных усилителях ОР1.1, ОР1.2 и ОР2.1 собран входной инструментальный усилитель с коэффициентом усиления около 40 dB (100 раз) имеющий высокое входное сопротивление и большое подавление синфазной помехи, наводимой на электроды и сигнальные провода (в основном это 50 Гц от сетевого напряжения 220 В). Для её дополнительного подавления на входах инструментального усилителя стоят двойные Т-образные мосты, настроенные на частоту 50 Гц. Эти фильтры, совместно с R1, R2 и фильтрами низких частот R10C8 и R11C9 понижают входное сопротивление каскадов до 100-200 кОм и делают его зависимым от частоты, но это не критично влияет на получаемый результат поэтому была выбрана именно такая простая схемотехника. К тому же, принудительное понижение входного сопротивления позволило уменьшить внутренние шумы ОР1.1, ОР1.2 на инфранизких частотах.
Рис.5
С выхода элемента ОР2.1 сигнал проходит через ФНЧ R22C15 и ещё один заграждающий активный Т-образный мост на 50 Гц собранный на ОР2.2 и далее через фильтр высоких частот C19R31 поступает на OP3.1. Фильтр C19R31 служит для уменьшения коэффициента усиления на частотах ниже 10 Гц, что в некоторой мере выравнивает итоговое усиление в полосе частот 4. 20 Гц до +/- 1,5 dB. С выхода OP3.1 снимается сигнал, усиленный ещё на 24 dB (15-16 раз). После OP3.1 происходит режекция частоты 100 Гц двойным мостом C22R36C24R35C23R37 и конечная коррекция амплитудно-частотной характеристики полосы пропускания на элементе OP3.2. На R38, R42 и S2 собран переключатель режимов «ЭЭГ» и «ЭКГ». На самом деле это обыкновенный делитель, который в режиме показаний «ЭКГ» ослабляет выходной сигнал примерно в 10 раз, соответствуя разнице уровней, указанных на таблице рисунка 1. После переключателя режимов стоит переменный резистор для плавной регулировки уровня сигнала, поступающего в звуковую карту. На схеме показан конденсатор С27 – он устанавливается для «развязки» по постоянному уровню при подключении прибора к компьютеру через микрофонный вход. Приклеен термоклеем к корпусу, а выводами припаян к контакту резистора и выходному разъёму «J». При использовании линейного входа звуковой карты его можно не устанавливать. Резисторы R38 и R42 марки МЛТ-0,25 установлены на контактах S2.
На цифровой микросхеме IC1 собран калибровочный генератор, служащий для указания на диаграммах уровня входного сигнала, равного 50 мкВ. При нажатии кнопки S1 генератор выдаёт на 10 ножке микросхемы прямоугольные импульсы частотой около 10 Гц, которые, пройдя через цепь R12C15 сильно искажаются и становятся похожими на треугольник (или «пилу»). В принципе, менять вид импульсов не обязательно и С12 можно намного уменьшить или убрать.
Детали, в большинстве своём, применялись SMD-шные типоразмера 0805. Конденсаторы в двойных Т-образных мостах, по крайней мере, в первых трёх, нужно ставить с небольшим температурным коэффициентом ёмкости (ТКЕ). Совсем не плохи из широкодоступных оказались простые китайские плёночные зелёного цвета (рис.6).
Рис.6
Под них и разведена программой печатная плата (рис.7) размерами 65х33 мм. При её изготовлении по лазерно-утюжной технологии изображение надо зеркалить.
Рис.7
Ёмкость конденсаторов и резисторов мостов обязательно подбирать перед пайкой и, конечно, проверять уровень подавление каскадов, уже впаяв детали в плату. Для подгонки номиналов можно применять параллельное и последовательное включение деталей. Частоты подавления мостов желательно немного (хотя бы на доли герца) разнести от центральной частоты 50 Гц. Это даст некоторую гарантию работоспособности прибора при изменении частоты сетевого напряжения плюс-минус 1 Гц.
Конденсаторы С13 и С14 набраны из SMD-шных большой ёмкости — на старых компьютерных платах часто встречаются такие конденсаторы на 10-15 мкФ. В крайнем случае, вместо них можно поставить электролитические танталовые или оксидные, но это не совсем корректно.
Операционные усилители применялись NE5532 и LM833 в корпусах SOIC−8. LM833 работают на частотах ниже 10 Гц намного лучше (шумят меньше). Для дополнительного уменьшения уровня шумов на первый операционник «бутербродом» напаян ещё один такой же. Измерений, насколько стало лучше, не проводил, но визуально было видно, что низкочастотных флуктуаций стало меньше, а теоретически шум должен уменьшаться в 1,42 раза.
Калибровочный генератор был спаян на кусочке макетной платы, поэтому файла разводки нет. Микросхема К561ЛЕ5 заменяема без переделки схемы на К561ЛА7. Частота генерации подбирается ёмкостью конденсатора С2. Генератор можно собрать и на других элементах (например, транзисторах) главное, чтоб частота была в районе 10-20 Гц.
На передней панели прибора установлены: сетевой переключатель марки B100G, рассчитанный на 250 В и 3 А; светодиод индикации «Сеть»; резистор регулировки уровня выходного сигнала СП3-4б; кнопка «Калибровка» – КМ2-1 или подобную; переключатель режимов «ЭЭГ-ЭКГ» — МТ-1 или П2Т-1-1В. Сигнальные входные разъёмы «Электрод 1» и «Электрод 2» – RCA гнёзда, выходное – аудио гнездо 3,5 мм (моно или стерео, не важно). Ещё один разъём (BANANA с закруткой) для электрода «земля» установлен на заднюю стенку прибора и соединён проводом МГТФ с платой (рис.7) в районе входных сигнальных контактов. Так же на задней стенке в держателе ДПБ крепится и предохранитель на ток 0,5-1 А.
Все входящие и выходящие в печатную плату провода крепятся пайкой. Но сигнальные контакты по входу и выходу разведены с шагом 2,54 мм, чтоб при желании можно было поставить двухштырьковые гребёнки PLS. Питание микросхем заведено максимально близко к ОР1, а уже от него перемычками расходится к ОР2 и ОР3 (красные линии на рисунке 7).
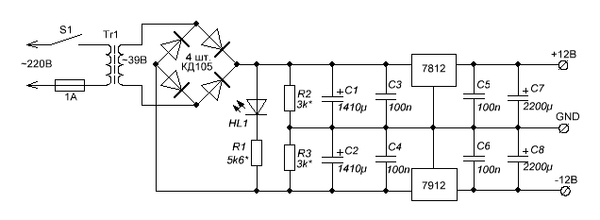
В блоке питания можно применить любой маломощный трансформатор с одной вторичной обмоткой на напряжение от 25 до 40 вольт, как на рисунке 8, или с двумя раздельными обмотками на 12-20 вольт с соответствующей коррекцией схемы. Основная задача – обеспечить малый уровень пульсаций выходных напряжений при токах нагрузки около 50 мА.
Рис.8
Диоды выпрямителя – КД105, можно любые другие на напряжение более 100 В и ток более 300 мА. Сопротивление резистора R1 для светодиода HL1, индицирующего работу прибора, выбирается для обеспечения тока через него около 5-10 мА. Конденсаторы С1 и С2 составлены из трёх параллельно соединённых 470,0 мкФ, рассчитанных на напряжение 35 В. Конденсаторы С7 и С8 должны быть большой ёмкости и если место в корпусе позволяет, то лучше набрать из нескольких хотя бы 8 000 — 10 000 мкФ. Стабилизаторы напряжений можно применить как слаботочные, так и мощные. Лучше, конечно, мощные. Особенно, если конденсаторы по выходу стоят большой ёмкости. Напряжение питания не критично – работа прибора проверялась как при шестивольтовом двуполярном напряжении, так и при пятнадцативольтовом. Ещё более высокое напряжение потребует введения цепи ограничения питания для цифровой микросхемы IС1.
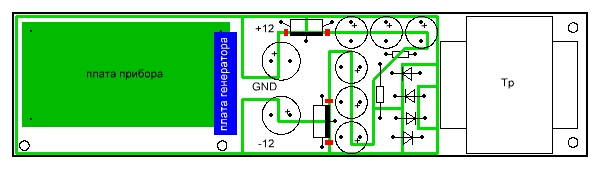
Плата блока питания выполнена из фольгированного с двух сторон стеклотекстолита размерами 45х180мм и служит основой для крепежа трансформатора и плат самого прибора и генератора. Нижняя сторона подключена к массе и используется как экран, а на верхней вырезаны проводящие дорожки и к ним припаяны детали блока питания. На рисунке 9 показано их примерное расположение. Красным помечены smd конденсаторы 100нФ С3, С4, С5 и С6. Плата калибровочного генератора установлена вертикально.
Рис.9
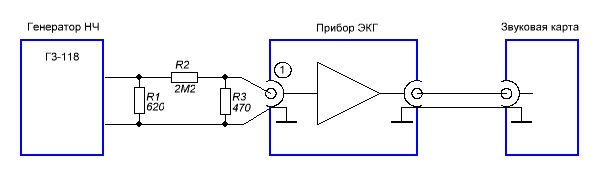
После сборки платы и проверки её работоспособности нужно настроить генератор калибровочного уровня. Сначала надо собрать делитель -73 dB из резисторов сопротивлениями 2,2 МОм и 470 Ом (рис.10). Если на вход такого делителя подать с генератора звуковой частоты (можно с компьютера) сигнал двойной амплитудой 0,223 В, то на его выходе будет 50 мкВ, которые надо подать на один из входов прибора. Запускаем программу SpectraLAB, допустим, в режиме осциллографа, и запоминаем уровень синусоиды на графике. Затем отключаем входной разъём, нажимаем кнопку «Калибровка» и резистором R15 выставляем такой же уровень, что был при сигнале с генератора.
Рис.10
Корпус прибора склеен эпоксидным клеем из МДФ панелей толщиной 6 мм.
В качестве электродов, снимающих биопотенциалы, можно применять как стандартные медицинские, так и самодельные, сделанные из подручных средств. Все приведенные ниже примеры были сняты с датчиков, электроды которых изготовленных из рублёвых монет. Для обеспечения лучшего контакта с телом человека под монетки подкладывались кусочки ваты, смоченные соленой водой. При использовании медицинских электродов и специального геля (электродного контактного вещества) [1] показания становятся более выраженными и стабильными.
Для самостоятельного изготовления электродов потребуется два полутораметровых хорошо экранированных провода и один двухметровый (можно не экранированный), два штекера RCA, две монетки, канцелярский зажим, термоклей и изолента (или термоусадочная трубка). Каждый экранированные провод с одной стороны стандартно припаивается к штекеру RCA, а с другой разделывается так, чтоб после пайки центрального проводника к монетке оплётка не касалась её поверхности. Для этого и нужна изолента. А чтоб монетка не оторвалась, место пайки и часть провода заливается термоклеем (рис.11).
Рис.11
Двухметровый провод – это для изготовления электрода «земля». Он с одной стороны просто оголяется для закрутки в разъёме BANANA, что на задней панели прибора, а к другому концу припаивается канцелярский зажим (рис.12), которому надо немного ослабить усилие сжатия.
Рис.12
В целях электробезопасности при проведении измерений корпус компьютера должен быть заземлённым. Если питание к нему подходит по двухпроводной схеме, то на корпусе системного блока всегда присутствует половина сетевого напряжения – это особенность импульсного блока питания. В таком случае надо проводить от распределительного щита до компьютера отдельный провод «земля» или искать другой способ заземления. По этой же причине, если используется ноутбук, то он НЕ ДОЛЖЕН находиться на подзарядке во время проведения измерений.
Теперь несколько примеров работы прибора
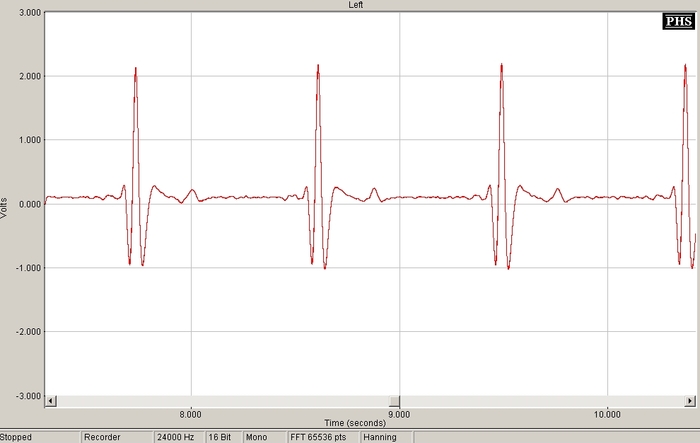
Самое простое – снятие электрокардиограммы (сердце) на рисунке 13. Электроды «1» и «2» закреплены на груди. Один — около солнечного сплетения, другой ближе к подмышечной области. Электрод «земля» – на запястье правой руки. Импульсы большие и красивые. Человек, близкий к медицине, посмотрев на скриншот, сказал, что видно почти все зубцы, и в принципе, зная положение электродов, можно даже проводить некоторый анализ данных.
Рис.13
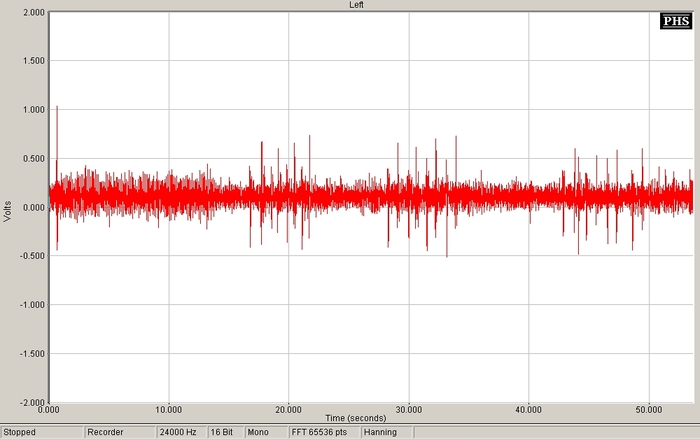
На рисунке 14 пример снятия электромиограммы (или электроокулограммы – тут я не разобрался 🙂 ). Скорее всего, показаны импульсы мышечной активности при движении яблоками глаз. Электроды «1» и «2» закреплены на левой и правой височных областях, а общий электрод – на мочке правого уха.
Рис.14
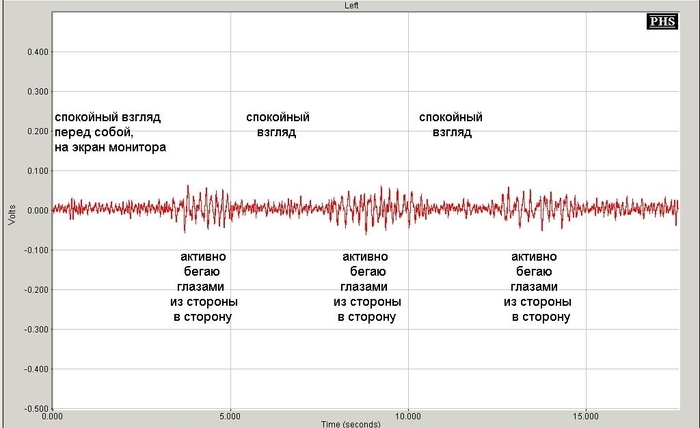
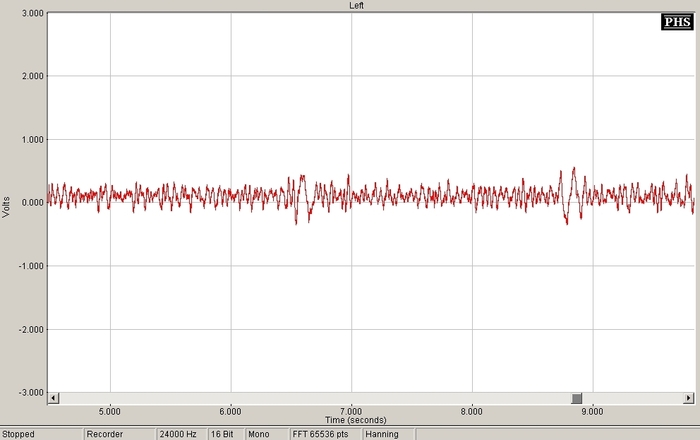
Рисунок 15. Такое же движение глазами, с электродами на тех же местах, как и при вышеприведённом скриншоте, но более общий вид. В начале записи (левая четверть экрана – 12-14 секунд) видно включение калибровочного сигнала 25 мкВ. Затем идут поочерёдно паузы и движение глазами влево и вправо.
Рис.15
Рисунок 16. Другая электромиограмма с электродами на тех же местах, но более подробно и без подключения провода «земля». Сначала неподвижно смотрю направо (или налево, уже не помню). Затем делаю движение глазами влево — это импульс между шестой и седьмой секундами. Затем идёт пауза, а перед девятой секундой виден импульс от движения глазами направо. Насколько смог разобраться, импульсы имеют разную полярность, т.е. проинвертированны.
Рис.16
Скриншоты выглядят по-разному, потому что были сделаны в разное время и, скорее всего, на разных приборах. Было изготовлено ещё два подобных устройства, в основном предназначенных для контроля ЭКГ, поэтому немного отличались схемотехникой. Один с LC фильтр-пробками после инструментального усилителя, другой с заграждающими мостами Вина-Робинсона и без фильтрации сигналов по входу. Последний вариант хоть и получился самый габаритный (с воздушным двухсекционным переменным конденсатором, да и собран был на макетной плате с обыкновенными, выводными деталями), но понравился больше всего – у него широкая рабочая полоса, есть возможность перестраивать частоту режекции в пределах +/- 1,5 Гц и регулировать добротность фильтра, вырезая всего 5-10 Гц из всей полосы пропускания. Максимально регистрируемая частота в такой версии выбирается установками частоты дискретизации в программе SpectraLAB (или SpectraPLUS) – при установке значения «Sampling Rate» равному 12 кГц максимально оцифровываемая частота не может быть выше 6 кГц.
Если описанный прибор использовать как электрокардиограф, то к выходу последнего операционного усилителя можно подключить компаратор со светодиодом. Закрепив светодиод на передней панели или на другом видном месте, по его вспышкам можно визуально контролировать частоту пульса человека.
Так же все принимаемые с прибора сигналы можно не только просматривать, но и прослушивать как обыкновенный звук.
Во вложении — схемы в формате программы Splan7, плата в формате Sprint-Layout 5.0 , расчётный файл АЧХ прибора для программы RFSim99 и wav запись ЭКГ для программы SpectraPLUS.
Если возникли вопросы, пишите на адрес sibmon@yandex.ru. Постараюсь с ответом не затягивать, но оперативности не гарантирую – в сети бываю редко. Только не надо задавать вопросы по медицинской тематике – пособие [1] я так и не осилил… 🙂
Андрей Гольцов, r9o-11, г. Искитим, 2013-2014.
источник
Электромиография
Электромиография — это метод изучения биоэлектрических процессов, развивающихся в мышцах людей и животных во время различных двигательных реакций. Метод основан на записи биопотенциалов скелетных мышц. Запись колебаний мышечных потенциалов (рис.) производится специальными приборами — электромиографами различных типов.
Хотя электромиограммы отражают только колебания потенциалов, которые развиваются непосредственно в мышце, все же по их качественным и количественным особенностям можно судить также о нормальном или патологическом состоянии ЦНС, регулирующей все виды двигательной активности человека. При различных заболеваниях возникают разнообразные нарушения нормальной картины электромиограммы (рис.).
При миогенных нарушениях (миозиты, миопатии) отмечаются асинхронные колебания с высокой частотой, укорочение длительности колебаний. В случаях далеко зашедших миогенных атрофии имеется снижение амплитуды колебаний.
При денервации мышцы появляются патологические виды колебаний:
низковольтные (чаще двух- и трехфазные) потенциалы фибрилляций.
При сегментарных ядерных парезах и амиотрофиях (поражение двигательных клеток ствола головного и спинного мозга) наблюдается снижение электрической активности, иногда до «биоэлектрического молчания», появление редких колебаний потенциалов фибрилляций.
При надсегментарных расстройствах (центральные параличи, гиперкинезы) выявляется снижение амплитуды колебаний в ЭМГ пораженных мышц, асинхронность возбуждения двигательных клеток и мышечных волокон.
Сопоставление электромиографических и клинических данных позволяет уточнить место (локализацию) и тяжесть повреждения нервной системы и мышц. Сравнение повторно записанных в одной и той же мышце электромиограмм помогает обнаружить улучшение (при выздоровлении) ее функционального состояния или ухудшение (при прогрессирующем заболевании), а также служит одним из оснований для объективной оценки результатов проводимого лечения.
Электромиографические данные могут оказать существенную помощь при диагностике ранних стадий заболевания и при легких повреждениях нейромоторной системы: возникающие в таких случаях двигательные расстройства иногда бывают столь незначительны, что клиническое обследование их еще не обнаруживает, тогда как электромиограммы, зарегистрированные высокочувствительным аппаратом, уже отражают патологически измененную электрическую активность мышц.
Электромиографию широко используют не только в неврологической клинике, но и при других заболеваниях человека (сердечно-сосудистых, онкологических, инфекционных и др.).
Электромиография (от греч. mys, myos — мышца, grapho — записываю) — регистрация электрических потенциалов; скелетных мышц. Электромиографию используют как метод исследования нормальной и нарушенной функции двигательного аппарата человека и животных. Электромиография включает методики по изучению электрической активности мышц в состоянии покоя, при произвольных, непроизвольных и вызванных искусственными раздражениями сокращениях.
С помощью электромиографии изучают функциональное состояние и функциональные особенности мышечных волокон, двигательных единиц, нервно-мышечной передачи, нервных стволов, сегментарного аппарата спинного мозга, а также надсегментарных структур; изучают координацию движений, выработку двигательного навыка при различных видах работы и спортивных упражнениях, перестройку работы пересаженных мышц, утомление. На основании электромиографии создан метод управления биотоками мышц, который нашел практическое применение при управлении так называемыми биоэлектрическими протезами (см. Протезирование).
Электромиограмма — кривая, получаемая на фотобумаге, фотопленке или на бумаге при регистрации электрических потенциалов скелетных мышц. Она может быть записана с помощью специального прибора, получившего название электромиограф, или других приборов, используемых для регистрации биопотенциалов. Прибор, как правило, имеет не менее двух каналов записи. Каждый канал включает в себя отводящие электроды, усилитель биопотенциалов и регистрирующее устройство. В большинство электромиографов предусматривается устройство для зрительного и слухового контроля (рис. 1).
Рис. 1. Схема устройства прибора для электромиографии.
Основным источником колебаний электрического потенциала мышц является распространяющийся по мышечным волокнам процесс возбуждения. Однако, поскольку электромиограмма регистрируется в области двигательных точек (см. Электродиагностика), часть электрического потенциала составляет потенциал, возникающий при возбуждении концевых пластин. Электрические потенциалы скелетных мышц можно отводить внутриклеточно или внеклеточно.
Внутриклеточное отведение электрических потенциалов отдельных мышечных волокон у человека позволяет определять те характеристики, которые раньше изучались при микроэлектродных исследованиях на животных или препаратах: величины мембранных потенциалов мышечных волокон, деполяризацию и гиперполяризацию мембран и т. п. (см. Биоэлектрические явления). Регистрацию внутриклеточных потенциалов скелетных мышц ряд авторов называет внутриклеточной электромиографией.
Внеклеточное отведение электрических потенциалов проводят двумя методами:
1) при помощи электродов с относительно малой отводящей поверхностью (сотые доли квадратного миллиметра), погружаемых в мышцу посредством игл (рис. 2, 1—3); при этом во всех случаях, кроме униполярного отведения, оба отводящих электрода находятся на небольшом расстоянии друг от друга (как правило, менее 0,5 мм); 2) при помощи электродов с относительно большой отводящей поверхностью (30— 100 мм 2 ), обычно помещенных на кожу над мышцей на сравнительно большом расстоянии друг от друга (1—2 см) (рис. 2, 4—6). В первом случае принято говорить о «локальном», во втором — о «глобальном» отведении. «Локальное» отведение позволяет изучать электрические потенциалы, возникающие в небольшом объеме мышечной ткани: потенциалы отдельных двигательных единиц, суммарные потенциалы небольшого количества двигательных единиц, в условиях патологии — потенциалы отдельных мышечных волокон. Основным объектом изучения является двигательная единица. Это понятие первоначально означало совокупность мышечных волокон, иннервируемых одним мотоневроном.
Рис. 2. Игольчатые и накожные электроды для регистрации электромиограмм: 1 — концентрический; 2 — биполярный; 3 — мультиэлектрод (по Бухталу); 4 — 6 — накожные электроды различных типов.
Рис. 3. Колебания потенциала мышцы при «локальном» отведении:1 — потенциал двигательной единицы; 2 — потенциал мышечного волокна (потенциал фибрилляции); 3 — положительный денервационный потенциал; 4 и 5— полифазные потенциалы (по Бухталу); в — ритмические разряды двух двигательных единиц.
В настоящее время многие авторы под двигательной единицей понимают совокупность функционально объединенных мышечных волокон, работающих как единое целое. Почти одновременное возникновение возбуждения в мышечных волокнах двигательной единицы приводит к тому, что возникают колебания потенциала, отражающие возбуждение двигательной единицы в целом (потенциалы двигательной единицы). Для исследования потенциалов двигательных единиц обычно используют концентрический электрод (рис. 2, 1). Биполярные электроды (рис. 2, 2) значительно искажают начальную и конечную часть потенциала двигательной единицы.
При «локальном» отведении учитывают форму, длительность и амплитуду потенциала отдельной двигательной единицы и тип электромиограммы (рис. 3). Форма потенциала двигательной единицы двухфазная или трехфазная с преимущественно выраженной отрицательной фазой; примерно в 3% случаев встречаются полифазные потенциалы. Длительность потенциала двигательных единиц зависит от их структуры. Она, как правило, больше в мышцах с крупными двигательными единицами и меньше в мышцах с мелкими двигательными единицами. Например, в четырехглавой мышце бедра и передней большеберцовой мышце, где имеются крупные двигательные единицы, включающие до 1500—2000, а иногда и более мышечных волокон, средняя длительность потенциала двигательной единицы у взрослых составляет 10—15 мсек, а в мышцах глаза, двигательные единицы которых имеют 5—10 мышечных волокон,— всего 1 — 3 мсек. Длительность потенциала двигательной единицы увеличивается с возрастом, например в возрасте 10 лет для передней большеберцовой мышцы она равна 9,7 мсек, 30 лет — 12,3 мсек, 60 лет — 15,2 мсек. Амплитуда колебаний потенциала двигательной единицы зависит от большего или меньшего удаления электрода от активных мышечных волокон и может достигать 3—5 мВ, однако средние величины значительно меньше — порядка 200 мкв. В расслабленной мышце биопотенциалы не регистрируются. При слабом сокращении мышцы потенциалы двигательной единицы следуют друг за другом в виде не строго ритмического ряда примерно одинаковых по амплитуде колебаний. Для мышц конечностей количество разрядов двигательных единиц в одну секунду принимается равным 5—10 при слабом сокращении, 20—30 при среднем по силе сокращении и 50—60 при сильном сокращении. Частота разрядов двигательных единиц в мелких мышцах обычно выше, чем в крупных (в мышцах глаза достигает 150—200 в 1 сек).
Увеличение силы сокращения мышц происходит как за счет увеличения частоты повторных возбуждений отдельных двигательных единиц, так и за счет вовлечения в работу новых двигательных единиц. Соответственно меняется тип «локально» отведенной электромиограммы. Различают три основных ее типа: потенциалы отдельной двигательной единицы, смешанный и интерференционный. При слабом сокращении регистрируются или потенциалы отдельной двигательной единицы (1-й тип), или потенциалы многих двигательных единиц, среди которых обычно можно выделить потенциалы отдельной двигательной единицы (2-й тип). При среднем по силе и сильном сокращениях регистрируется интерференционная электромиограмма, в которой практически невозможно выделить потенциалы отдельных двигательных единиц (3-й тип). О синхронности разрядов двигательных единиц наиболее точно получают сведения, используя мультиэлектроды. По данным «локального» отведения, степень синхронизации разрядов двигательных единиц при слабых сокращениях мышц у здоровых незначительна; она стойко повышается при некоторых поражениях спинного мозга (см. ниже электромиография в клинике). Данные «глобального» отведения, позволяющего изучать электромиограмму при длительных и максимальных по силе сокращениях мышц, говорят о значительном повышении у здоровых синхронизации разрядов двигательных единиц при утомлении и некоторых режимах работы мышц.
Потенциалы отдельных мышечных волокон можно зарегистрировать только при денервации мышцы, когда двигательные единицы перестают существовать как функциональное целое и отдельные мышечные волокна начинают «спонтанно» возбуждаться. Это так называемые потенциалы фибрилляций, которые имеют длительность 0,5 — 3 мсек и амплитуду 50—200 мкв.
«Глобальное» отведение позволяет изучать колебания электрических потенциалов, возникающих в большом объеме мышечной ткани, содержащей обычно сотни двигательных единиц. Как правило, эти потенциалы отражают сумму потенциалов многих двигательных единиц; поэтому электромиограмму при «глобальном» отведении часто называют суммарной, хотя при некоторых обстоятельствах при «глобальном» отведении могут регистрироваться и потенциалы отдельных двигательных единиц. Для «глобального» отведения, помимо накожных электродов, можно применять обычные иглы; в условиях эксперимента используют вживленные электроды в виде серебряных пластинок, подшитых к мышце. В большинстве случаев применяют биполярное или униполярное отведение накожными электродами. Униполярный способ отведения оправдывает себя в физиологии спорта. В клинике в настоящее время используют почти исключительно биполярное отведение. При нем отводящие электроды располагаются на расстоянии 1—2 см друг от друга так, чтобы один находился над двигательной точкой, а другой — дистальнее или оба над двигательной точкой. Обычно отводящие электроды постоянно фиксированы на изолирующей пластинке. В соответствии с запросами клинической электромиографии разработана специальная схема обследования здоровых испытуемых и больных (Ю. С. Юсевич). Эта схема предусматривает обязательную регистрацию биопотенциалов симметричных мышц в покое, т. е. во время максимального произвольного расслабления мышц, при различных пробах, ведущих к непроизвольному изменению напряжения мышц, и при произвольных их сокращениях. У здоровых испытуемых в хорошо расслабленных мышцах или не выявляется никаких колебаний потенциала, или выявляются низкоамплитудные колебания, которые рядом авторов считаются проявлением тонуса мышцы. При позно-тонических и произвольных сокращениях мышц электромиограмма представлена нерегулярными колебаниями различной амплитуды, формы и длительности. При слабом сокращении регистрируются более редкие и неравномерные по амплитуде колебания потенциала, при сильном сокращении возрастают частота следования и амплитуда колебаний. Увеличение амплитуды колебаний при увеличении статического напряжения показано на рис. 4. Частота следования колебаний может быть разной в различных мышцах, а также в одних и тех же мышечных группах у разных испытуемых. В среднем частота следования колебаний при максимальном по силе сокращении составляет 100—150 в 1 сек. Амплитуда колебаний зависит от многих условий: развития мышц, их состояния, выраженности подкожного жирового слоя (особенно при выраженных случаях ожирения) и в большой степени от выбора электродов. Амплитуда колебаний при максимальном по силе сокращении может достигать 4—6 мВ. Однако обычно регистрируются меньшие величины (рис. 5). Частота следования колебаний потенциала и амплитуда колебаний изменяются при изменении синхронизации разрядов двигательных единиц. Увеличение синхронизации при утомлении и некоторых режимах работы мышц ведет к уменьшению частоты следования колебаний и увеличению амплитуды.
Рис. 4. Электромиограмма двуглавой мышцы плеча при статическом напряжении различной силы (разная нагрузка).
Рис. 5. Электромиограммы, записанные при максимальном по силе сокращении правого (верхняя кривая) и левого (нижняя кривая) поверхностного сгибателя пальцев (биполярное отведение накожными электродами площадью 0,5 см 2 с расстоянием между центрами электродов 20 мм).
Большое количество ценных сведений о состоянии различных звеньев двигательного аппарата позволяет получить регистрация биопотенциалов мышцы при электрическом раздражении нервных стволов и мышечных волокон. Регистрация электромиограммы при раздражении мышечных волокон электрическим током позволила определить в норме и патологии скорость распространения возбуждения по мышечным волокнам, а при раздражении нервных стволов — состояние нервно-мышечной передачи, скорость распространения возбуждения по двигательным нервным волокнам, а также изучить моно- и полисинаптические рефлексы.
Помимо общей визуальной оценки, применяется и математическая обработка электромиограмм. Более широкое распространение получила оценка общей площади электромиограммы за единицу времени при помощи интеграторов и машинная обработка для проведения аутокорреляционного и особенно кросскорреляционного анализа.
источник